
近日,CDE最新公示消息,又一批藥品擬納入優(yōu)先審評(píng)。包括百濟(jì)神州的替雷利珠單抗、信達(dá)首款小分子抗癌新藥pemigatinib片、協(xié)和麒麟的First-in-classCCR4抑制劑莫格利珠單抗等在內(nèi)。
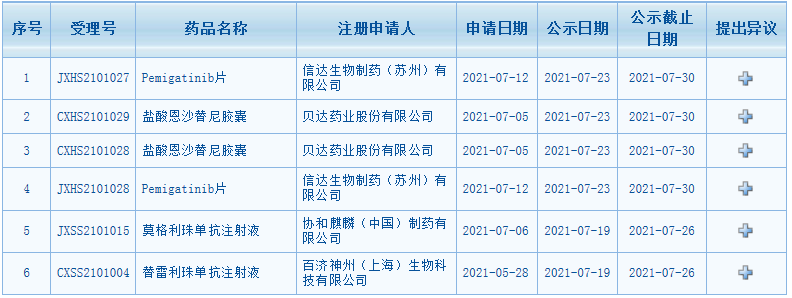
圖片來(lái)源:CDE
基石藥業(yè)艾伏尼布
艾伏尼布(Ivosidenib)是一款first-in-class、具有選擇性的、針對(duì)IDH1基因突變癌癥的強(qiáng)效口服靶向抑制劑。2018年7月獲得FDA批準(zhǔn)上市,成為全球首個(gè)且唯一一個(gè)獲得FDA批準(zhǔn)治療攜帶易感IDH1突變的成人復(fù)發(fā)或難治性急性髓系白血病(R/RAML)藥物。FDA還分別在2018年和2019年向此藥授予了用于急性髓細(xì)胞性白血病和膽管癌的孤兒藥稱號(hào)及突破性療法。
信達(dá)首款小分子抗癌新藥pemigatinib片
Pemigatinib屬于纖維細(xì)胞生長(zhǎng)因子受體(FGFR)亞型1/2/3的強(qiáng)效選擇性口服抑制劑。據(jù)藥智數(shù)據(jù)藥品注冊(cè)時(shí)光軸顯示,pemigatinib申報(bào)上市被NMPA受理到納入優(yōu)先審評(píng)僅僅只用了11天時(shí)間,適應(yīng)癥為既往至少接受過(guò)一種系統(tǒng)性治療,且經(jīng)檢測(cè)確認(rèn)存在有FGFR2融合或重排的晚期、轉(zhuǎn)移性或不可手術(shù)切除的膽管癌成人患者的治療。

貝達(dá)藥業(yè)鹽酸恩沙替尼
鹽酸恩沙替尼是一種新型強(qiáng)效、高選擇性的新一代ALK抑制劑,是貝達(dá)藥業(yè)和控股子公司Xcovery共同開發(fā)的全新的、擁有完全自主知識(shí)產(chǎn)權(quán)的創(chuàng)新藥;是貝達(dá)藥業(yè)在肺癌領(lǐng)域繼EGFR-TKI后的又一重大布局產(chǎn)品,有望成為首個(gè)由中國(guó)企業(yè)主導(dǎo)在全球上市的肺癌靶向創(chuàng)新藥。
協(xié)和麒麟的First-in-classCCR4抑制劑莫格利珠單抗
莫格利珠單抗注射液(Mogamulizumab)是抗CC趨化因子受體4(CCR4)單克隆抗體,是由協(xié)和發(fā)酵株式會(huì)社研發(fā),并已相繼在日本和美國(guó)上市。近日,這款First-in-classCCR4抑制劑在中國(guó)申報(bào)上市被受理,并快速納入擬納入優(yōu)先審評(píng)名單,適用于既往接受過(guò)至少一次全身性治療的蕈樣肉芽腫(MF)或Sézary綜合征(SS)成人患者的治療。數(shù)據(jù)顯示,蕈樣真菌病占所有皮膚淋巴瘤的50%-70%,它能夠?qū)е吗W的紅疹和皮膚傷口,且可擴(kuò)散到身體其它部位;塞扎里綜合癥則是影響血液和淋巴結(jié)的一種罕見皮膚淋巴瘤;MF的白血病階段,與紅皮病相關(guān)聯(lián),約占皮膚T細(xì)胞淋巴瘤的3%。

百濟(jì)神州百澤安擬納入優(yōu)先審評(píng)
7月19日,CDE官網(wǎng)顯示,百濟(jì)神州PD-1抗體替雷利珠單抗上市申請(qǐng)擬納入優(yōu)先審評(píng),適應(yīng)癥為適用于既往經(jīng)治的局部晚期不可切除或轉(zhuǎn)移性高度微衛(wèi)星不穩(wěn)定型(MSI-H)或錯(cuò)配修復(fù)缺陷型(dMMR)實(shí)體瘤。
信息與數(shù)據(jù)來(lái)源:藥智數(shù)據(jù)、CDE、企業(yè)官網(wǎng)、企業(yè)公告等公開數(shù)據(jù)與信息。

 冀公網(wǎng)安備 13010802000997號(hào)
冀公網(wǎng)安備 13010802000997號(hào) 微信掃一掃
微信掃一掃